国家食品药品监督管理总局于5月27日公布《药品、医疗器械产品注册收费标准》和《药品注册收费实施细则(试行)》、《医疗器械产品注册收费实施细则(试行)》,调整了药品注册收费标准,制定了医疗器械新的收费标准。
新的收费标准是根据国家发改委、财政部《关于重新发布中央管理的食品药品监督管理部门行政事业性收费项目的通知》和《关于印发〈药品、医疗器械产品注册收费标准管理办法〉的通知》进行制定的。
药品、医疗器械注册收费是国际通行做法。国家受理生产企业的药品、医疗器械注册申请和开展审评、审批,需花费大量人力、物力,这部分成本应当由申请者支付,由全体纳税人负担这部分费用是不公平的。
此前,我国药品注册收费标准由国家发改委、财政部1995年制定,医疗器械产品注册未收费。由于社会工资水平、物价上涨等原因,收费标准已经严重偏低。以2013年审批国产新药的收费标准为例:澳大利亚98万元(人民币),加拿大176万元,美国1207万元,日本185万元,我国只有3.5万元。
这次收费标准的调整,是按照成本补偿原则确定的。根据国家发改委、财政部规定的测算原则和授权,总局聘请第三方会计师事务所,进行了药品、医疗器械产品注册费成本的测算,确定了新的收费标准。新标准虽然有了大幅度提高,但与国际上一些国家的收费标准相比依然较低。仍以新药注册收费为例,调整后的国产新药注册申请收费标准为62.4万元,仅相当于澳大利亚的64%、加拿大的35.5%、美国的5.2%,日本的33.7%。
按照现行的财务制度,注册收费收入全额上缴中央和地方国库,开展审评审批工作所需经费通过同级财政预算统筹安排。
附 件:药品、医疗器械产品注册收费标准
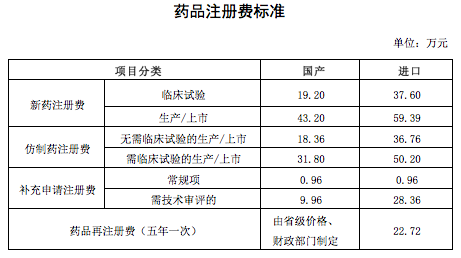
注: 1.药品注册收费按一个原料药或一个制剂为一个品种计收,如再增加一种规格,则按相应类别增收20%注册费。
2.《药品注册管理办法》中属于省级食品药品监督管理部门备案或国务院食品药品监督管理部门直接备案的药品补充申请事项,不收取补充申请注册费,如此类申请经审核认为申请内容需要技术审评的,申请人应按照需要技术审评的补充申请的收费标准补交费用。
3.申请一次性进口药品的,收取药品注册费0.20万元。
4.进口药品注册收费标准在国内相应注册收费标准基础上加收国内外检查交通费、住宿费和伙食费等差额。
5.港、澳、台药品注册收费标准按进口药品注册收费标准执行。
6.药品注册加急费收费标准另行制定。
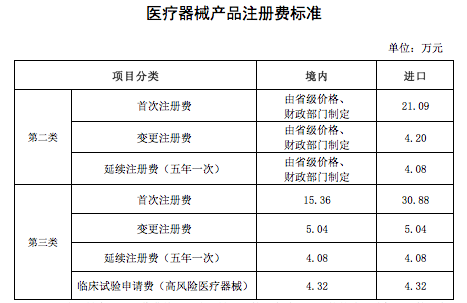
注: 1.医疗器械产品注册收费按《医疗器械注册管理办法》、《体外诊断试剂注册管理办法》确定的注册单元计收。
2.《医疗器械注册管理办法》、《体外诊断试剂注册管理办法》中属于备案的登记事项变更申请,不收取变更注册申请费。
3.进口医疗器械产品首次注册收费标准在境内相应注册收费标准基础上加收境内外检查交通费、住宿费和伙食费等差额。
4. 港、澳、台医疗器械产品注册收费标准按进口医疗器械产品注册收费标准执行。
5. 医疗器械产品注册加急费收费标准另行制定。